مرحبا بك في هذا المنتدى !
يبدو أنك جديد هنا. إذا كنت تريد أن تتورط، انقر فوق أحد هذه الأزرار!
روابط سريعة
الأقسام
- 9.5K جميع الأقسام
- العلوم الطبية الأساسية Basic Medical Sciences
- علم التشريح العام و الجنين Anatomy and Embryology
- علم وظائف الأعضاء (الفيزيولوجيا) Physiology
- علم النسج Histology
- علم النسج العام ( عدا الأسنان ) General Histology
- علم النسج الخاص بالأسنان Oral histology
- علم الخليةو الحياة Biology
- علم التشريح المرضي Pathology
- التشريح المرضي العام ( عدا الأسنان ) Pathology
- التشريح المرضي الخاص بالأسنان Oral Pathology
- علم الأحياء الدقيقة Microbiology
- الجراثيم و الفيروسات Germs and Viruses
- الطفيليات الطبية Parasitology
- الفطور و الحشرات Insects and Fungi
- علم الوراثة الطبية Medical Genetics
- علم المناعة الطبية Medical Immunology
- 4 العلوم الطبية السريرية Clinical Medical Sciences
- الأمراض الداخلية Internal Medicine
- 4 الجراحة Surgery
- التوليد و الأمراض النسائية Gynacology & Obstetrics
- الصحة الجنسية Sexual Health
- طب الأطفال Pediatrics
- الجلدية Dermatology
- العينية Ophthalamology
- انف و أذن و حنجرة Ear, Nose, and Throat
- الطب المخبري labratory Medicine
- علم الأورام Oncology
- الطب الشرعي Forensic Medicine
- الطب النفسي Psychiatric
- التغذية والطب البديل Nourishments and Alternative Medicine
- طب الطوارئ و الإسعافات الأولية Emergency Medicine And Primary aids
- متلازمات طبية Medical Syndromes
- علم الأشعة Radiology
- طب الأسنان Dental Medicine
- التعويضات المتحركة الكاملة و الجزئية Removable Prothodontics
- المداواة الترميمية operative dentistry
- المداواة اللبية Endodontics
- طب أسنان الأطفال Pediatric Dental
- جراحة الوجه والفكينoral surgery
- التعويضات الثابتة Fixed Prothodontics
- المواد السنية dental materials
- النسج حول السنية periodontology
- التقويم Orthodontics
- منتدى فنيي الأسنان dental technicians
- طب الفم العام general oral medicine
- علم الأشعة Radiology
- حالات سريريةClinical Cases
- أخر مستجدات طب الأسنان last news
- المنتدى الطبي السني العامgeneral dentistry
- علم الصيدلة Pharma
- علم الأدوية
- علم الأدوية Pharmacology
- أدوية الطوارئ Emergency drugs
- المضادات الحيوية Antibiotics
- الأدوبة المسببة للتشوهات الجنينية Teratogenic drugs
- أدوية Drugs
- علم الكيمياء Chemistry
- كيمياء حيوية سريرية Clinical Biochemistry
- الكيمياء العامة و العضوية و الفيزيائية General & organic chemistry & physical
- الكيمياء الحيوية Biochemistry
- الكيمياء التحليلية و التحليل الآلي Analytical chemistry and the automated analysis
- علم عقاقير Pharmacognosy
- الطب البديل Alternative Medicine
- علم الأعشاب الصيدلانية Pharmaceutical Herbs
- التكنولوجيا الصيدلية Pharmatical technology
- الصيدلانيات Pharmaceutics
- الصيدلة الحيوية والحرائك الدوائية Biopharmaceutics & Pharmacokinetics
- الصناعة الدوائية Drug Industry
- علم السموم Toxicology
- الوصفات الطبية Prescriptions
- صيدلية المجتمع و أدوية OTC Medicines OTC
- الكيمياء الصيدلية Pharmaceutical chemistry
- الصيدلة سريرية و صيدلية المشافي Clinical & Hospital Pharmacy
- دمويات و مناعيات hematology & immunology
- مراقبة جودة الأدوية Drug Quality Control
- البيولوجيا الجزيئية Molecular Biology
- الصحة العامة و تلوث البيئة General Health
- المنتدى الصيدلاني العام
- الجودة الغذائية Food quality
- قسم الجودة الطبية Department of Medical Quality
- قسم الجودة العام General Quality Department
- قسم السلامة والصحة المهنية Department of Occupational Safety and Health
- قسم جودة وسلامة الأغذية Department of Food Quality and Safety
- المنتدى الطبي العام
- المنتدى الطبي العام
- منتدى العلوم والتكنولوجيا الطبية Medical Technology
- قانون و أخلاقيات المهنة
- تاريخ و آداب الطب
- الدراسات العليا و الدراسة في الخارج
- امتحانات Medical Exams
- تبادل الكتب الطبية و الميديا و البيانات الطبية
- مواضيع طبية غير مصنفة
- قسم الأسرة و المجتمع
- العناية بالمرأة الحامل و المرضع
- تربية الأطفال
- الصحة العامة
- التغذية الصحية و الغذاء الصحي
- أسريات
- 2 استراحة العيادة السورية
- المنتدى العام
- نشاطات و ترفيه
- 1 إسلاميات
- تطوير الذات و البرمجة اللغوية العصبية NLP
- المنتدى التقني
- مكتبة الصور و التصميم
- 1 المنتدى الثقافي و الأدبي
- المنتدى الرياضي
- منتدى اللغات Foriegn Languages
- الساحة العامة
- ساحة الحوار و النقاش
- ترحيب و تعارف
- قسم الاستشارات الطبية
- البحوث والندوات العلمية
- الاقتراحات و التطويرات
- الأقــســـام الــعـــامــة
- منتدى الحوار العام
- المواضيع العامة القديمة المستردة
- المواضيع الحاوية على مرفقات
الرئيسية › علم الصيدلة Pharma › علم الكيمياء Chemistry › الكيمياء التحليلية و التحليل الآلي Analytical chemistry and the automated analysis
المعايرات الحمضية الأساسية باستخدام الناقلية الكهربائية1
تم تعديل 2009/02/15 في الكيمياء التحليلية و التحليل الآلي Analytical chemistry and the automated analysis
الناقلية (1)
المعايرات الحمضية الأساسية باستخدام الناقلية الكهربائية
-1 معايرة محلول ( Hcl ) بماءات الصوديوم (0.01N) :
- أ -نأخذ (10ml) من حمض كلور الماء و نمدد بدورق (100ml) حتى العلام بالماء المقطر و نجانس المحلول و من ثم ننقل المحلول إلى بيشر و نضع ا لمسرى الخاص بجهاز الناقلية فيه ثم نضيف حجوما من (NaoH) الموجود في السحاحة بمقدار (2ml) ونسجل الناقلية عند كل إضافة كما في الجدول التالي :
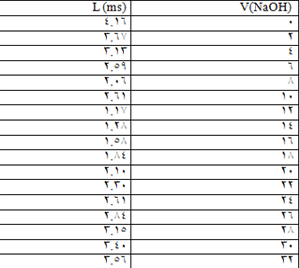
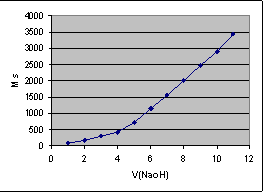
نرسم العلاقة الخطية لتغيرات الناقلية بدلالة الحجم المضافV (NaOH)
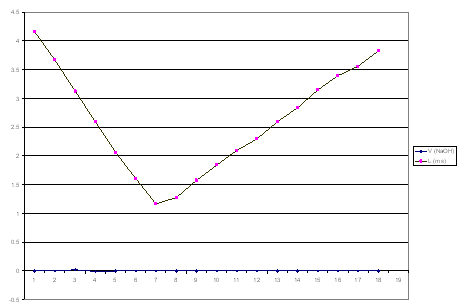
- نلاحظ أن V(NaOH)اللازم للوصول لنقطة التكافؤ هو : V2 = 7 ml
- نحسب تركيز حمض الـ HCl :
( N1 . V1 ) HCl = (N2 . V2 )NaOH
( N1 . 10 )HCl = ( 0.01 . 7 ) NaOH
N1 = 0.01 . 7 / 10 = 0.007 N
NHCl = N1 . 10 = 0.007 . 10 = 0.07 N الأصلية
التجربة (2)
نأخذ (5ml) من حمض كلور الماء و نمدد بدورق (100ml) حتى العلام بالماء المقطر و نجانس المحلول و من ثم ننقل المحلول إلى بيشر و نضع ا لمسرى الخاص بجهاز الناقلية فيه ثم نضيف حجوما من (NaoH) الموجود في السحاحة بمقدار (2ml) ونسجل الناقلية عند كل إضافة كما في الجدول التالي :

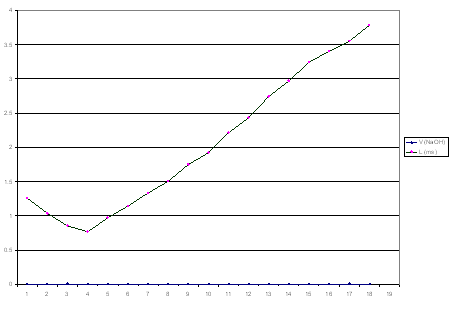
العلاقة الخطية لتغيرات الناقلية بدلالة الحجم المضافV (NaOH)
-نلاحظ أن الحجم اللازم للوصول لنقطة التكافؤ V 2 = 4 ml
- نحسب تركيز حمض الـ HCl :
( N1 . V1 ) HCl = (N2 . V2 )NaOH
( N1 . 5 )HCl = ( 0.01 . 4 ) NaOH
N1 = 0.01 . 4 / 10 = 0.004N
NHCl = N1 . 20 = 0.004 . 20 = 0.08 N الأصلية
معايرة محلول ( CH3COOH ) بماءات الصوديوم ((0.01N
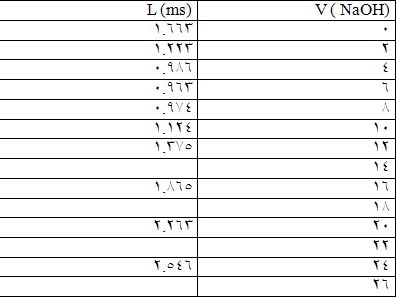
أ -نأخذ (10ml) من حمض الخل و نمدد بدورق (100ml) حتى العلام بالماء المقطر و نجانس المحلول و من ثم ننقل المحلول إلى بيشر و نضع ا لمسرى الخاص بجهاز الناقلية فيه ثم نضيف حجوما من (NaoH) الموجود في السحاحة بمقدار (1/2ml) ونسجل الناقلية عند كل إضافة كما في الجدول التالي :
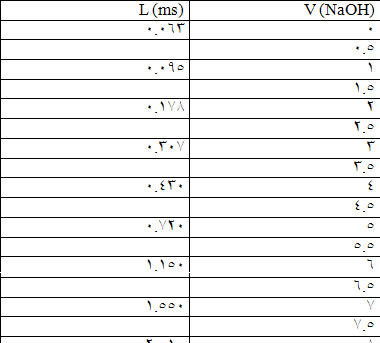
نرسم العلاقة الخطية لتغيرات الناقلية بدلالة الحجم المضاف V (NaoH) فيظهر منحني نسقط نقطة انعطافه على محور السينات فيكون الحجم الناتج
هو حجم V (NaoH) اللازم للوصول لنقطة التكافؤ:
ج – نحسب تركيز حمض (CH3COOH) المجهول من قانون المعايرة :
NaoH(N2.V2 ) =CH3COOH (N1.V1)
0.01 * V (eq) = N1 * 10
N1 * 10 = 0.01 *4
N 1 =0.004
0.01 * V (eq) = N1 * 10
N1 * 10 = 0.01 *4
N 1 =0.004
ونوجد N CH3COOH ونضربه بعدد مرات التمديد n=20
NCH3COO =N1 . n الأصلية
= 0.004*20
= 0.08 N
= 0.004*20
= 0.08 N
3معايرة مزيج حمضي ( Hcl + CH3COOH ) بماءات الصوديوم (0.01N) :
أ -نأخذ (5 ml) من حمض كلور الماء و(5 ml) من حمض الخل نمدد بدورق (100ml) حتى العلام بالماء المقطر و نجانس المحلول و من ثم ننقل المحلول إلى بيشر و نضع ا لمسرى الخاص بجهاز الناقلية فيه ثم نضيف حجوما من (NaoH) الموجود في السحاحة ونسجل الناقلية عند كل إضافة كما في الجدول التالي :
ب – نرسم العلاقة الخطية لتغيرات الناقلية بدلالة الحجم المضاف V (NaoH) فيظهر منحني عليه نقطتي انعطاف نسقط نقطة الانعطاف الأولى على محور السينات فيكون الحجم الناتج هو حجم
V (NaoH) اللازم لمعايرة الحمض الأقوى و نسقط النقطة الثانية و بطرح الحجم الثاني من الأول نحصل على حجم V (NaoH) اللازم لمعايرة الحمض الأضعف
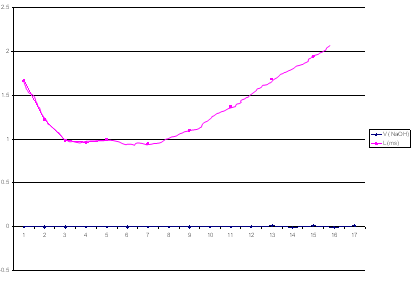
V1 = 3.5
هو حجم (NaoH) اللازم لمعايرة الحمض الأقوى ( HCl)
V2 = 7
فيكون:
V2 - V1 = 7 – 3.5 = 3.5
هو حجم (NaoH) اللازم لمعايرة الحمض الأضعف ( حمض الخل)
- نحسب تركيز حمض (HCl) المجهول من قانون المعايرة :
( N1 . 10 ) HCl = (0.01 . 3.5 )NaOH
N1 = 0.01 . 3.5 / 10 = 0.0035N
عدد مرات التمديد = 20 مرة
NHCl = N1 . 20 = 0.0035 . 20 = 0.07 N الأصلية
- نحسب تركيز حمض (CH3COOH) المجهول من قانون المعايرة
NaoH(N2.(V2-V1) ) = CH3COOH (N1.V1)
N 1 . 10 = 0.01 ( 3.5)
N1 = 0.0035N
NCH3COOH = N1 . 20 = 0.0035 . 20 = 0.07 N الأصلية
التعليقات