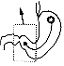|
فسيولوجيا المعدة والاثناعشر PHYSIOLOGY OF THE STOMACH AND DUODENUM أهم وظائف المعدة والاثناعشر هي الإفراز والحركة. يتناول الإنسان طعامه في خلال دقائق، وتستقبله معدته التي تقوم بدور مخزن الطعام، ثم تطلقه المعدة خلال ساعات إلى الاثناعشر بعد تعرضه للهضم بالحمض والأنزيمات. ومع ذلك، فإن أهم وظيفة للمعدة ليست كيمائية بل آلية؛ إذ تحطم كتل الطعام الصلبة إلى جزئيات صغيرة قبل أن يُطْلِقَ غارُ المعدة سراحَها. وفي الاثناعشر، تتم معادلة باها pH الطعام الممزوج مع إفرازات المعدة الذي يدعى بالكيموس chyme، بإفرازات الاثناعشر والبنكرياس التي تحتوي على البيكربونات bicarbonate، وتتم أيضا معايرة أسمولية osmolarity الكيموس مع البلازما. إضافة إلى ما تقدم، تقوم الغـُـذَيـَّـاتِ nutrients بتنبيه الخلايا الصُم الواقعة في الغشاء المُبَطـِّـنِ للاثناعشر للإفراج عن عديدات الببتيد polypeptides، وهذه تعدل النشاط الإفرازي والحركي للسبيل الهضمي. وسرعة توريد الكيموس من المعدة إلى الاثناعشر تعتمدً على أُسمولية الكيموس ومحتوياته من الدهن والسكريات، وذلك من خلال عمل مستقبلات receptors خاصة في الغشاء المبطن للجزء العلوي من الاثناعشر (هانت* Hunt). إفراز عصارة المعدة Secretion of gastric juice تتكون عصارة المعدة بشكل رئيسي من الببسين pepsin والعامل الداخلي intrinsic factor والشوارد ومذابات solutes عضوية أخرى في حمض الهيدروكلوريد المخفف. وقد تم الاعتراف تقليديًا بثلاث مراحل لإفراز عصارة المعدة وهي: المرحلة الرأسية Cephalic. وتتم من خلال نشاط العصب المبهم vagal activity إما نتيجة الإثارة النفسية كما بين بافلوف* Pavlov، أو نتيجة إثارة بمنعكس reflexly عن طريق تنبيه غار المعدة (أوفناس*). المرحلة المعدية Gastric. الجاسترينات gastrins عبارة عن عديدات الببتيدات، وهي مختلفة في قدرتها على حث الإفراز وأوزانها الجزيئية، ولكنها متطابقة في وظائفها (جريجوري*)، وتتحرر الجاسترينات من خلايا ج G-cells الغَارِيّة استجابةً للانتفاخ الآلي لغار المعدة، أو استجابة لوجود بروتينات اللحم. وبعد تحريرها من خلايا ج، تصل الجاسترينات عن طريق الدوران المجموعي systemic circulation إلى الخلايا الجدارية. ويجري التحكم بإفراز الحمض بواسطة تغذية راجعة سلبية negative feedback؛ فعندما ينقص الـ باها pH داخل المعدة نتيجة إفراز الحمض إلى ما دون 3، يتم إثباط تحرير الجاسترين. ويبقى نتاج الحمض مرتفعًا، ولمدة نصف ساعة بعد الأكل، وذلك بسبب التأثيرات الدارئة buffering effect للوجبة الممزوجة. ودور الهستامين، الذي عرف منذ أمد بعيد بقدرته على تنبيه إفراز المعدة الحمضي، ما زال مثيرًا للجدل، لكن يبدو في الوقت الحاضر أن الجاسترين والأسيتايل كولين يعملان على الخلايا الجدارية، بواسطة إطلاق الهستامين، وبالتلاحم مع الشَوَادِّ agonist والضواد antagonist المنظـِّـمة الأخرى. المرحلة المعوية Intestinal phase. كان يعتقد أن إطالة إفراز الحمض لبضع ساعات بعد تناول الطعام، مردُّه لوجود عوامل معوية intestinal factors. أما الآن فيبدو أن عدم التفريغ التام للوجبة الممزوجة من المعدة ولعدة ساعات يسبب (على الأرجح وبشكل رئيسي)، تنبيهًا آليًا وكيماويًا لغار المعدة الذي يقوم بدوره بإفراز الجاسترين لمدة طويلة. والتأثير المباشر لوجود الكيموس في الأمعاء مثبط في أكثره ويهدف للإبقاء على حياد الـ باها pH في الاثناعشر. وتسبب حمضنة الاثناعشر تحرر السيكريتين secretin الذي يقوم بدوره بإثباط إفراز المعدة للحمض (جروسمان*). وهناك عديدات ببتديد معوية أخرى من المرجح أن تنخرط في هذا التنظيم. إفراز الببسين Pepsin secretion إفراز الببسين في العادة مقترن بإفراز شاردة الهيدروجين H+، ولكنه قد يكون مختلفا بسبب المنبهات كولينية الفعل cholinergic أو بسبب الهرمونات عديدات الببتيد polypeptide hormones. مخاط المعدة Gastric mucus يغطي الغشاء المبطن للمعدة ويزلـِّقه إفراز لزج مكون من عديدات السكريد المخاطية mucopolysaccharides. وكما هو الحال في البيبسين، فإن إفراز المخاط، قد يثار بتنبيه العصب المبهم نتيجة تناول الطعام. وال باها pH في الغشاء المخاطي للمعدة قلوي alkaline وله قدرة دَرْءٍ buffering كبيرة (قد تصل إلى 80 مليمول/لتر، هولاندر*). ويُكَوِّنُ مخاط المعدة مانعـًا فسيولوجيًا يقي غشاءها من الإصابة الآلية وتأثير حمض المعدة. هذا ويمكن تقوية هذه الوظيفة الواقية بإفراز كميات قليلة من البيكربونات إلى داخل طبقة المخاط، مما يخلق مدروجـًا لـ باها pH gradient. وقد اقترح دافينبورت* تحطم هذا المانع في حالات قرحة المعدة، مما يؤدي إلى الانتشار المعاكس لشوارد الهيدروجين H+ ions إلى داخل خلايا الغشاء المخاطي. وهذا الاقتراح، قد يفسر، ولو جزئيًا، سبب نقص إفراز حمض المعدة عند هؤلاء المرضى. كما أن نقص عدد الخلايا الجدارية عند هؤلاء المرضى قد يسبب نقص إفراز الحمض عندهم. وقد يتأذى المانع بسبب أحماض الصفراء المجزورة refluxed عبر البواب، أو بسبب العقاقير مثل الساليسيلات salicylate والكحول. أما تهيج غشاء المعدة، فقد يؤدي إلى فائض في إنتاج المخاط. إفراز الاثناعشر الخارجي Duodenal exocrine secretion بالرغم من قصر أنبوب الاثناعشر النسبي، إلا أن المساحة السطحية للاثناعشر واسعة جدًا، وذلك نتيجة لترتيب الغشاء المبطن للاثناعشر على شكل ثنايا مستعرضة التجعدات الصمامية valvulae conniventes (صمامات الرَفَّةwinking valves ). هذا ويتم إنتاج (الإفرازات القلوية) في الجزء الأول والثاني من الاثناعشر بواسطة غدد برونر* التي تصب في خبايا ليبركن* crypts of Lieberkuhn، ويتناسب حجم الإفراز مع كمية الحمض التي يتم توريده عبر البواب. ويقوم الإفراز القلوي بدرجة كبيرة بتصويب وضع الـ باها pH إلى درجة التعادل.
إفراز المعدة والاثناعشر الصَمَّاوِي Gastric and duodenal endocrine secretion إن كميات عديدات البيبتيد واختلاف أنواعها، تجعل من العدل القول بأن السبيل الهضمي alimentary tract أكبر عضو غدي صمـاوي في الجسـم. وبالـرغم من أن السكـريتين secretin كــان أول هـرمون وصـف وظيفـيـًا مـن قبـــل بيليـس* وستارلنج*، إلا أن التقدم الذي شهدناه في مجال المقايسة المناعية immunoassay والكيمياء الخلوية cytochemistry وكيمياء البروتينات، قد أدى إلى اكتشاف غالبية الهرمونات المعدية المعوية خلال عشر السنوات الأخيرة. وبالرغم من أن وظائف هذه الهرمونات غير مؤكدة، إلا أن هناك بعض الحقائق المتفق عليها.
بنية عديدات الببتيد Structure of polypeptides اعتمادا على بنية عديدات الببتيد، يمكن تقسيم غالبيتها إلى قسمين رئيسيين. فالجاسترين والكولسيستوكاينين-بانكريوزايمين (CCK.PZ) ذات ألفة بنيوية ووظيفية مع سلسلات أحماض أمينية انتهائية مشابهة، وعديدا الببتيد كلاهما موجودان عند الإنسان بأنواع مختلفة باختلاف طول سلسلة الأحماض الأمينية النهائية. أما السكريتين والجلوكاجون المعوي enteroglucagon والببتيد المعوي الفعال في الأوعية الدموية vaso-active intestianl peptide (VIP) والببتيد المعدي المثبط gastric inhibitory peptide (GIP) فلها ألفة بنيوية عديدة. غير أن بعض عديدات الببتيد مثل الموتلين motilin يبدو أن لها بنية فريدة.
التوضُّع Localisation تتبعثر الخلايا التي تفرز هرمونات عديدات الببتيد بين الخلايا الظهارية للغشاء المخاطي المبطن للمعدة والأمعاء، ولا تتجمع هذه الخلايا على شكل غدد متميزة. وينحصر إفراز أغلب الجاسترين بغار المعدة gastric antrum؛ ويفرز ما تبقى منه في الأمعاء الدقيقة، خاصة في الاثناعشر. وتحاذي الخلايا المفرزة للهرمونات لـُمْعَةَ القناة الهضمية، وفي بعض الحالات، تم التعرف على منبهات لـُمَعِـيـَّة luminal stimuli تستثير إطلاق عديدات الببتيد. وتوجد عديدات الببتيد في الأعصاب العضلية المعوية myenteric nerves، وادعي بوجود أعصاب بيبتونية الفعل peptidergic nerves (بولاك Polak). وتمّ التعرف أيضًا على أغلب عديدات الببتيد التي توجد طبيعيـًا في الأمعاء داخل عصبونات الجهاز العصبي المركزي.
الوظيفة Function يبدو أن معظم عديدات الببتيد ذات علاقة بتنظيم الإفرازات الهضمية الخارجية، إما باستثارة هذه الإفرازات أو إثباطها: يستثير الجاسترين إفراز حمض المعدة ويستحث كل من السكريتين والـكوليسيستوكينين بانكريوزايمين CCK-PZ إفرازات البنكرياس، بينما يقوم بإثباط إفراز حمض المعدة كل من السكريتين والببتيد مثبط المعدة GIP، والببتيد المعوي الفعال في الأوعية الدموية VIP، والسوماتوستاتين والجلوكاجون. وتمارس عديدات الببتيد دورًا رئيسًا آخر، وهو السيطرة على النشاط الحركي للمعدة والأمعاء، فيؤدي الكوليسيستوكينين بانكريوزايمين CCK-PZ إلى تقلص المرارة، بينما ينبه الجاسترين النشاط الحركي للمعدة، وقد يؤثر الببتيد المطلق للجاسترين (البومبيسين bombesin في الثدييات) على النشاط الحركي للمعدة، من خلال تأثيره المركزي على العصب المبهم. وقد وصفت عدة تأثيرات في النشاط الحركي، ولكن لم تظهر الصورة جلية بعد. ويوحى قرب الخلايا الصم من الخلايا خارجية الإفراز الخاصة بها، والمؤثرة في عملها، بأن التأثير عن طريق الجوار (Paracrine) (عبور عديد الببتيد من الخلايا المفرزة إلى الخلايا التي تعتبر هدفًا لها عن طريق الانتشار الموضعي) قد يحدث فعلاً، غير أنه يصعب إثبات ذلك، ولم يتوافر الدليل القاطع على حدوثه. إضافة لما تقدم، فإن من المحتمل أن تعمل عديدات الببتيد كناقلات عصبية neurotransmittors، أو منسقات عصبية neuromodulators في داخل الضفائر العصبية الداخلية intrensic nerve plexus للمعي.
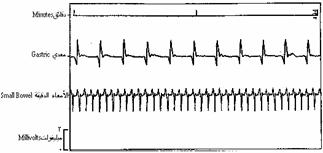
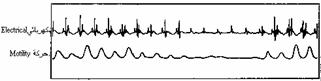
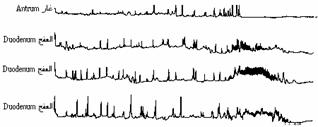
النشاط الحركي للمعدة والاثناعشر Gastroduodenal motor activity يتطلب تعاقبُ خطوات الهضم والامتصاص العاملة على الغُذَيَّات المتناولة، دفعًا منهجيًا لمحتويات اللـُمْعَة عبر مناطق مختلفة وبسرعة مختلفة، ويتم ذلك بتنظيم هرموني عصبي للنشاط التقلصي للعضلات الملساء التي تغلف جدار القناة الهضمية تغليفا تامـًا. والنشاط الحركي للمعدة والاثناعشر نظميٌّ rhythmic، وتسيطر عليه موجات من (ذبذبات) كهربائية تزيل الاستقطاب depolarize، وتعرف باسم الذبذبات البطيئة slow waves، ويتم توليد الذبذبات البطيئة في موقع ناظمة pacemaker علوية في المعدة والاثناعشر، وتنتشر الذبذبات بعيدًا عن الفم aborally عبر العضلات الطولانية الملساء، وبسرعة عدة سنتمترات في الثانية. ويبث ناظم المعدة الذي يقع في قاع fundus المعدة ثلاث ذبذبات في الثانية، وتتجه هذه الذبذبات إلى البواب، ولكنها لا تمر عبره. وتتولد ذبذبات الاثناعشر البطيئة من قبل ناظم يقع مباشرة تحت البواب وبسرعة مقدارها عشر ذبذبات في الدقيقة (هيرمون-تيلور*). وتعرف الذبذبات البطيئة المتواترة أحيانًا باسم التواتر الكهربائي الأساسي basic electric rhythm، وتشبه تخطيط كهربائية القلب في طبيعتها وعملها، ويبين تسجيل الذبذبات من على سطح مصلية serosa المعدة والاثناعشر تغيرات متواترة ومشابهة لتخطيط كهربائية القلب ولكنها بطيئة نسبيًا (الشكل44-4). ونظرا لأن انقباض العضلات الملساء الواقعة في أي مكان في السبيل الهضمي، يحدث فقط أثناء مرور الذبذبات البطيئة، فإن نشاط الناظم يتحكم بتوقيت حدوث النشاط الحركي، وباتجاهه، لإن الذبذبات البطيئة قابلة للاتجاه ذنبيـًا caudally فقط. ولكن، (وليس كحال تخطيط كهربائية القلب)، لا تسبب الذبذبات البطيئة حدوث تقلص كل مرة تمر بها، ويُبين التسجيل المتزامن للنشاط الكهربائي للاثناعشر مع تسجيل تغيرات الضغط داخل اللـُمْعَة (الشكل44-5)، وجود نشاط منظم للذبذبات البطيئة. ولكن تغيرات الضغط، تحدث فقط عند حدوث ذبذبات بطيئة مصحوبة باندفاع حاد مفاجىء spike bursts (الشكل 44-5). وتحدد التغيرات العصبية والهرمونية، الداخلية منها والخارجية، وهي غير معللة تعليلاً تامـًا في وقتنا الحاضر، إذا كانت الذبذبة البطيئة تؤدي إلى تقلص أم لا، وبواسطة هذه العوامل العصبية والهرمونية، تجري عملية التكامل بين النشاط الحركي للمعدة والأمعاء، مع خطوات الهضم والامتصاص.
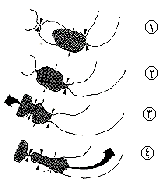
تفريغ المعدة Gastric emptying يتم إنجاز المزج والتفريغ البطيء لوجبة مخزونة من المعدة بواسطة ‘مضخة الغار antral pump’. وينبه تحريرالجاسترين النشاط الحركي للمعدة، وذلك بإحداث زيادة بسيطة في تكرار حدوث الذبذبات البطيئة، وبإحداث زيادة ملحوظة في النشاط التقلصي المصاحب للذبذبات البطيئة. وتدفع موجات التقلص المتجهة قاصيـًا محتويات المعدة باتجاه غار المعدة (الشكل 44-6). وعند امتلاء الغار، يفتح البواب، وليس للبواب توتر استراحي resting tone، ويسمح بمرور بعض الكيموس chyme. وعندما تصل موجة التقلص إلى البواب، يتقلص البواب، وبهذا تسبب موجات تقلص الغار المستمرة الاندفاع المعاكس لمحتويات الغار باتجاه جسم المعدة. وبهذا تتسبب كل موجة تقلص في إطلاق قليل من الكيموس ومزج ما تبقى من محتويات الغار. وبهذه الطريقة، لا يتم التغلب على قدرة الاثناعشر في استعادة الـ (باها pH) إلى درجة التعادل. ويعتمد حجم ما يفقده الغار عبر البواب عند كل تقلص على درجة اللزوجة، وكمية المواد الصلبة التي تحتويها المعدة، إذ تفرغ السوائل بسرعة أكبر.
مقارنة الصيام والإطعام feeding. Fasting vs هناك فرق ملفت للنظر بين مجمل النشاط الحركي للمعدة والاثناعشر أثناء الصيام وبعد الإطعام. ففي أثناء الصيام، هناك نشاط حركي نشيط لمدة دقائق قليلة، يعقبه غياب النشاط الحركي لمدة ساعة أو أكثر. وفي حال غياب الطعام من المعدة، يتكرر إلى ما لا نهاية حدوث دورات يتبادل فيها النشاط القصير مع العطالة inertia الطويلة. وهذا النمط ليس دوريًا فحسب، بل هو متنقل migratory. ويتزامن حدوث النشاط الحركي القصير الأمد في كل من المعدة والاثناعشر العلوي. وعندما يخبو النشاط آنف الذكر، تمر جبهة النشاط باتجاه قاصي تحت الاثناعشر، وهكذا دواليك، على طول الأمعاء الدقيقة (الشكل 44-7)، وبالمقارنة مع الذبذبات البطيئة، فإن سرعة تنقل النشاط الحركي آنفة الذكر بطيئة، ويستغرق مرورها من المعدة إلى نهاية اللفائفي terminal ileum ما بين ساعة إلى ساعتين، ويتصادف ظهور جبهة نشاط حركي جديدة في المعدة والاثناعشر مع وصول الجبهة السابقة إلى نهاية اللفائفي. ولقد تم وصف هذه المركبات complexes المتنقلة في العقد الأول من القرن العشرين باصطلاح تقلصات الجوع hunger contractions، ومن ثم جرى تغير الإصلاح حديثًا إلى مدبرة منزل المعي intestinal housekeeper (كود*)، وتهدف لدفع محتويات الأمعاء من الإفرازات والحطام. وبالمقارنة، ثانية مع نشاط الناظم، تقع ساعة ضبط جبهات الحركة في حالة الصيام خارج العضلة الملساء، وربما في الضفيرة العضلية المعوية. وللاثناعشر أهمية في تحقيق تكامل هذا النشاط، وهناك دليل على أن لأحد هرمونات الاثناعشر، موتيلين motelin، علاقة في عملية السيطرة والنشاط الحركي في حالة الصيام. وسرعة مرور جبهة ‘مدبرة منزل المعي’ عالية، لدرجة لا تسمح بإتمام عملية هضم وامتصاص الطعام، لذلك، تختفي هذه الموجات مباشرة مع الإطعام ويحل محلـَّها في مستوى الأمعاء نشاط تقلصي متقطع، يسمح بخضِّ الكيموس ومزجه من دون مرور سريع. وعندما تصبح المعدة خاوية، يستأنف النمط السريع من الحركة. ويسبب إعطاء الجاسترين حدوث تنبيه جزئي لتأثير الإطعام على نمط النشاط الحركي للمعدة (كود Code). ويبدو أن هناك احتمالاً بأن للهرمونات عديدات الببتيد المعدية والمعوية الأخرى علاقة في تنظيم النشاط الحركي. كما أن هناك احتمالاً لأن توضح دراسات أخرى بأن بعض المتلازمات الشائعة وغير المحددة، ويطلق عليها (متلازمة الأمعاء الوظيفية functional bowel syndrome) هي اضطرابات تنظيم هرموني عصبي.
اختبارات إفراز المعدة TESTS OF GASTRIC SECRETION 1. اختبار ذروة نتاج الحمض (بنتاجاسترين) Peak acid output test (pentagastrin). 2. اختبار الأنسولين (هولاندر) Insulin (Hollander) test، وقد جرى استبداله في الوقت الحاضر (انظر الشرح). 3. اختبار امضغ وابصق Chew and spit test.
اختبار ذروة نتاج الحمض Peak acid output (بنتاجاسترين). يتم قياس الإفراز الأساسي للحمض بعد مصِّ المعدة الصائمة لمدة ساعة ومن ثم يجرى اختبار بنتاجاسترين، حيث ينبه إفراز الحمض من المعدة لأعلى درجة باستعمال البنتجاسترين (بيبتافلون Peptavlon، زيميكا Zemeca). وللبنتجاسترين أعراض جانبية يمكن إهمالها. وتعطى جرعة بمقدار 6 ميكروغم/كغم وزن، عن طريق زرقة تحت الجلد أو زرقة عضليًا، وتجمع العينات كل 15 دقيقة خلال الساعة التالية، (انظر الجدول 44-1). وتؤخذ بعدها نتائج أعلى عينتين متلاحقتين، جمعتا على مدار 15 دقيقة لكل منهما، وتجرى معادلتها إلى درجة باهـا 7 (pH 7) وتضاف النتيجتان، وتضربان بالعدد 2: أما الرقم الناتج، فهو ذروة نتاج الحمض (PAOp)، ويعبَّر عنه بميليمول شاردة هيدروجين mmol H+ (بارون*). ويبين الجدول (44-1) القيم التي تم استخراجها في مختلف الحالات.
وقد لا يمكن الاعتماد إلا جزئيًا على هذه الاختبارات، إذا لم يتم إجراؤها من قبل باحثين متمرسين. ومع ذلك يمكن أن يستنتج منها أن المريض لايمكن أن يكون لديه حمض أقل مما تم رشفه. وقد يكون لديه كمية حمض أكبر. وإذا كانت التقنية خاطئة، فلا يمكن إدراك ذلك. إن لهذا الاختبار قيمة في تشخيص متلازمة زولنجر-إليسون (Zollinger-Ellison's (ZE) syndrome) (انظر الفصل 47). أما في حالات قرحة الاثناعشر فيمكن استعمالها كدليل مفيد لاختيار أفضل العمليات الجراحية لمعالجة المريض. فعلى سبيل المثال، تجرى عملية قطع العصب المبهم مع النزح إذا كانت النتيجة منخفضة، ويمكن أن تجرى عملية قطع العصب المبهم مع استئصال غار المعدة، أو استئصال المعدة الجزئي إذا كانت النتيجة مرتفعة. اللاكلوريدية Achlorhydria، يعني هذا التعريف عدم قدرة المعدة على إنتاج عصارة ذات باها أقل من 7 (PH less than 7)، حتى بعد أقصى درجات التنبيه. ويحدث مثل ذلك في حوالي 18 بالمائة من المرضى المصابين بسرطانات المعدة (بارون Baron). اختبار الأنسولين (هولاندر). (انظر اختبار امضع وابصق لاحقا). يعزى إفراز الحمض بعد حدوث نقص سكري الدم إلى التأثير المباشر للعصب المبهم على مجمل الخلايا الجدارية parietal cell mass. وإعطاء الأنسولين لمريض سبق أن أجريت له عملية قطع مبهم تام، لن يؤدي إلى زيادة نتاج الحمض. ونظرًا لحدوث وفيات عديدة أثناء هذا الاختبار، عزيت لانخفاض سكر الدم، فقد تم هجره لمصلحة اختبار ‘امضغ وابصق’، (انظر لاحقًا). اختبار امضغ وابصق Chew and split test. ويمكن الحصول على نتائج مماثلة بتحقيق تنبيه العصب المبهم من خلال استخدام تقنية امضغ وابصق. وبعد إدخال أنبوب أنفي معدي، يمضغ المريض وجبة، ولكن بدلاً من بلعها، يقوم ببصقها في وعاء. ويحلّل تركيز الحمض المرشوف من المعدة بطريقة مماثلة لما هو مستخدم في اختبار الأنسولين. الاستجابة المبكرة Early response. يعني ارتفاع تركيز الحمض في أثناء الساعة الأولى بمقدار 20 مليمول/لتر فوق الإفراز الأساسي أن قطع المبهم غير تام. وفي حال خلو الإفراز الأساسي للمعدة من الحمض، فإن زيادة تركيز الحمض بمقدار 10 مليمول/لتر يعتبر إيجابيًا. الاستجابة المتأخرة Delayed response. قد تحدث الزيادة في إفراز الحمض بين الساعة الأولى والثانية، ويعزى ذلك إلى أن تنبيه العصب المبهم قد تسبب في تحرير أو إطلاق الجاسترين. وقد يختفي ذلك بعملية استئصال الغار antrectomy، وتعني أن قطع المبهم غير تام. ويمكن للاستجابة المبكرة السالبة أن تتحول لاستجابة موجبة، بعد بضعة أشهر أو حتى سنوات، ولم تتضح بعد أهمية هذا التحول في الاستجابة. إضافة لما تقدم، فإن كلا من: منحني تحمل الجلوكوز glucose tolerance curve، وصورة شعاعية لحفرة النخامي pitutary fossa، ومستوى الكالسيوم والفسفور المصلي، ومستوى 17-كيتو ستيرويدات البول، قد تساعد في الكشف عن حالة صعبة ذات خلفية صماوية- (متلازمة عديدة الغدومات - الفصل 37). تقدير مستوى الجاسترين الدوراني Estimation of circulating gastrin. يتزامن ارتفاع مستوى الجاسترين الدوراني مع زيادة في إفراز حمض المعدة. وتتوافر تقنيات للمقايسة المناعية الشعاعية للجاسترين، وتستند المقايسة على الأسس التالية: تتم تنشئة مستضدات antigens نوعية للجاسترين، وتتنافس العينة البيولوجية (الحياتية) مع هرمون موسوم شعاعيـًا radiactive labelled للارتباط مع المستضد. ويقوم الجاسترين المتواجد في العينة بإحباط كمي لالتحام المستضد مع الهرمون الموسوم، وتحدد درجة الإحباط هذه مستوى الجاسترين في العينة، ولقد ثبت نفع نتائج هذه الأبحاث في تشخيص متلازمة زولنجر-إليسون Zollinger-Ellison's syndrome (الفصل 47).
اختبارات إفراز الاثناعشر TESTS OF DUODENAL SECRETION لا توجد اختبارات معيارية لإفرازات الاثناعشر، لكن قد تبين مراقبة الـ باها (pH) في الجزء العلوي من الاثناعشر هبوطـًا كبيرًا في الـ باها (pH) بعد تناول وجبة طعام، ويعزى ذلك لفرط إفراز الحمض المتزامن مع قرحة الاثناعشر.
اختبارات النشاط الحركي للمعدة والاثناعشر TESTS OF GASTRODUODENAL MOTOR ACTIVITY يمكن مراقبة تفريغ المعدة من المواد شبه الصلبة بعدة طرق، ولكن أكثرها وثوقـًا هي استعمال آلة تصوير جاما لمتابعة تفريغ وجبة بيض مخفوق، موسومة بالتكنيشيوم. هذا وقد تكون لهذا الاختبار فائدة لتقييم نتائج الجراحة المجراة على مخرج المعدة. * جاك نيلور هانت Jack Naylor Hunt، معاصر. أستاذ الفيسيولوجيا سابقـًا، هيوستن، تكساس، الولايات المتحدة الأمريكية. * إيفان بيتروفيتش بافلوف Ivan Petrovich Pavlov، ولد عام 1849. عالم فسيولوجيا روسي. * بورج كارل ماجنس أُوفناس Bِrje Karl Magnus Uvnنs، معاصر، أستاذ الفسيولوجيا، جامعة ستوكهولم، السويد. * روديريك الفريد جريجوري Roderic Alfred Gregory، معاصر. أستاذ كرسي هولت Holt للفسيولوجيا، جامعة ليفربول، انجلترا. * مورتون جروسمان Morton Grossman، 1919-1982. مدير مركز أبحاث القرحة، لوس أنجلوس، كاليفورنيا، الولايات المتحدة الأمريكية. * فريدريك هولاندر Frederick G.Hollander، معاصر. جراح، مستشفى ميرسي، سانديغو، الولايات المتحدة الأمريكية. * هوراس دافينبورت Horace Davenport، معاصر. أستاذ الفسيويولوجيا سابقًا، جامعة ميشيغان، آن أربر، ميتشيغان، الولايات المتحدة الأمريكية. * يوهان كونراد برونر Johann Conrad Brunner، 1653-1729. اختصاصي علم تشريح، بازل، سويسرا. * يوهان ناتنيال ليبركن Johann Nathanael Lieberkuhn، 1711-1756. اختصاصي علم تشريح، ألماني. * ويليام مادوك بيليس William Maddock Bayliss، 1860-1924. اختصاصي فسيولوجيا، مستشفى يونيفيرسيتي كوليج، لندن، إنجلترا. * إيرنست هنري ستارلنج Ernest Henry Starling، 1866-1927، اختصاصي فسيولوجيا، مستشفى يونيفيرسيتي كوليج، لندن، إنجلترا. * جون هيرمون-تيلور John Hermon-Taylor، معاصر. أستاذ الجراحة، مستشفى سانت جورج، لندن، إنجلترا. * تشارلز ف. كود Charles F. Code، معاصر. أستاذ فسيولوجيا متقاعد، مايو كلينيك، روتشستر، الولايات المتحدة الأمريكية. * جيرمي هيو بارون Jeremy Hugh Baron، معاصر. مستشار الأمراض الداخلية، مستشفى سانت تشارلز ومستشفى همرسميث، لندن، انجلترا.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||